Doğada binlerce organik molekül bulunuyor ve bunlardan bazıları yaşama karşı tehdit unsuru iken (aflatoksin gibi) bazıları ise bağışıklık sisteminin vazgeçilmezlerindendir (vücudumuza almamız gereken yirmi farklı amino asit gibi). Bu makalede bağışıklık sistemimizin vazgeçilmez antioksidanlarından biri olan glutatyon nedir sorusuna cevap vererek bu molekülün kimyasal yapısı ve özellikleri, stereoizomerizasyonu ve farmakolojik özelliklerini ele alacağım.
Glutatyon nedir ve nasıl keşfedildi?
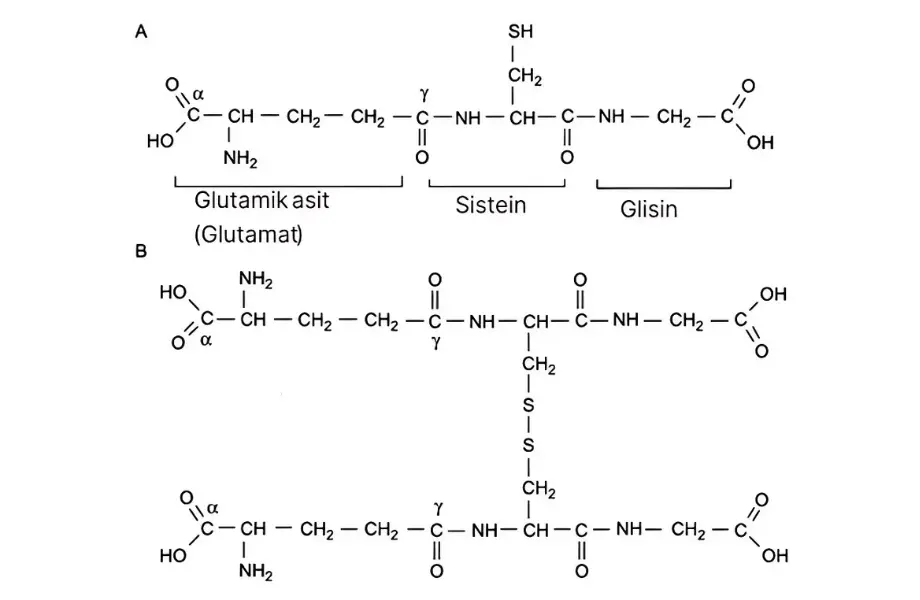
Glutatyon (C10H17N3O6S), birçok canlıda bulunan çok işlevli bir antioksidan biyomoleküldür. Glutatyon; glisin, sistein ve glutamik asit amino asitleri (bunlar, insan vücudunda bulunması gereken yirmi amino asitten üçüdür; bu da bize glutatyonun vücudumuz için ne kadar yararlı ve gerekli olduğunu gösteriyor) ve protein içermeyen bir tiyol grubundan oluşan antioksidan özellikte bir sülfür bileşiğidir. [1] [2] Üç amino asit içerdiği için tripeptid yapısındadır ve γ-glutamil-sisteinil-glisin bilimsel adıyla tarif edilir. [3]
Glutatyon ilk olarak 1888 yılında J. de Rey-Pailhade tarafından keşfedildi ancak isimlendirilmesi yıllar sonra oldu. [1] [5] 1921 yılında Cambridge Üniversitesi’nden Frederick Gowland Hopkins, kas dokusundan bir bileşik çıkardı ve bu bileşiğin çok yüksek ihtimalle glutamik asit ve sistein içeren bir dipeptid yapısı olduğunu söyledi. 1927 yılında bu söyleme karşı olarak bileşiğin aslında bir tripeptid olduğu iddia edildi ve (Hunters & Eagles, 1927; Non-Protein Sulfur Compounds of Blood: II. Glutathione) ve 1929 yılında glutatyonun Hopkins tarafından mayadan izole edilip incelenmesiyle bu kanıtlandı.
Hopkins ayrıca izole ettiği bu maddenin kırmızı kan hücrelerinde de bulunduğunu kaydetti. [1] [2] Günümüzde de bunun doğru olduğunu biliyoruz. Glutatyon gerçekten de alyuvarların sitozolünde, hemoglobin faaliyetleriyle gerçekleşen oto-oksidasyon olayları sonucu oluşan reaktif (tepkimeye girme eğilimi gösteren) oksijen türevlerine (EN: reactive oxygen species, ROS) karşı büyük rol oynuyor (Julia E. Raftos, Stephney Whillier,& Philip W. Kuchel, 2010). [5] [6] Buna sonradan tekrar değineceğim.
Tarihsel sürece geri gelirsek aynı yıl, Hopkins ve Hollandalı doktor Christiaan Eijkman, vitaminler (vital aminler) ve diğer beslenme faktörleri üzerinde yaptıkları çalışmalarla Nobel Fizyoloji veya Tıp Ödülü’ne layık görüldüler. [2]
Glutatyonun ilk sentezi ise 1952’de Cornell Tıp Koleji’nden kimyager Vincent du Vigneaud’a atfedilir. Du Vigneaud aynı zamanda 1955’te Nobel Kimya Ödülü’nü kazandı. Her ne kadar Nobel’i kazanmasının ana sebebi glutatyon molekülü olmasa da Du Vigneaud, biyolojik açıdan önemli sülfür bileşikleri üzerine çalıştı ve özellikle memelilerde cinsel birliktelik ve üreme olgularıyla ilişkilendirilen oksitosin üzerine yaptığı çalışmalarla dikkat çekti. Kendisi ayrıca 1953’te oksitosinin kimyasal yapısı tam olarak ayırarak protein yapılı bir hormonun tüm amino asit zincirini belirleyen ilk kişi oldu. [7]
Glutatyonun kimyasal özellikleri ve antioksidanlık
Glutatyon, üç büyük canlı aleminde de (bakteriler, arkeler ve ökaryotlar) en çok bulunan protein içermeyen tiyoldür. Görevleri çok ve önemli olduğundan yoğun olarak bulunur. Genelde sitoplazmada bulunur ancak duruma göre mitokondri, endoplazmik retikulum ya da peroksizomlarda da bulunabilir. Glutatyonun varlığı birçok canlının bağışıklığının önemli bir güvencesidir ve bu güvence glutatyonun antioksidan olma özelliğinden kaynaklanır.
Antioksidanlık, adından da anlaşılabileceği gibi “oksidanlık ve/veya oksidasyon karşıtı olma” anlamına gelir. Vücudumuzda hücre aktivitesi, çevresel etmenler (tütün kokusu, hava kirliliği, UV ışık, hava kirliliği), kimyasal süreçler için gerekli olan oksidasyon olayı ve bazı durumlarda egzersiz sonrasında [8] eşleşmemiş elektron bulunduran serbest radikaller ortaya çıkar. [8] [9] Yaşam için gerekli olmalarına karşın son derece reaktif de olan bu radikaller, canlının vücudundaki önemli moleküllerle (DNA, organeller veya diğer hücre yapıları gibi) tepkimeye girerek canlıya zarar verebilir. Antioksidanlar, bu eşleşmemiş elektronları eşleştirerek canlının zarar görmesini engellerler. [10]
Glutatyonun indirgenmiş halini (GSH) kullanarak çalışan glutatyon peroksidaz sadece serbest radikallerin değil aynı zamanda ağır metallerin, hidrojen peroksitlerin, DNA peroksitlerin ve ksenobiyotiklerin de zararlı etkilerini engelleyen bir enzimdir. [1] [4] [5] [9] Hücre metabolizmasını destekler, toksik stresi azaltır ve hücreye direnç sağlarlar.
Glutatyonun tepkimeleri
Glutatyon biyosentezi, ATP’ye bağımlı 2 basamaktan oluşur. İlk olarak, L- glutamat ve sistein öncülünden γ-glutamil-l-sistein ligaz aracılığıyla γ-glutamilsistein sentezlenir. Bu reaksiyon aynı zamanda glutatyon sentezinde hız sınırlayıcı basamaktır. İkinci olarak, Glutamilsistein’in C-terminaline glisin eklenir. Bu reaksiyon, glutatyon sentaz tarafından katalize edilir. [3] [4] Bu tepkimeler zinciri çoğu canlıda aynı işler ve ikinci basamağa geçilirken γ-ECS denilen bir ara madde kullanılır. Yapılan çalışmalarda bu maddenin yaşa bağlı bozukluklarda ve Alzheimer hastalığı gibi kronik hastalıklarda koruma sağladığı da görülmüş. [11]
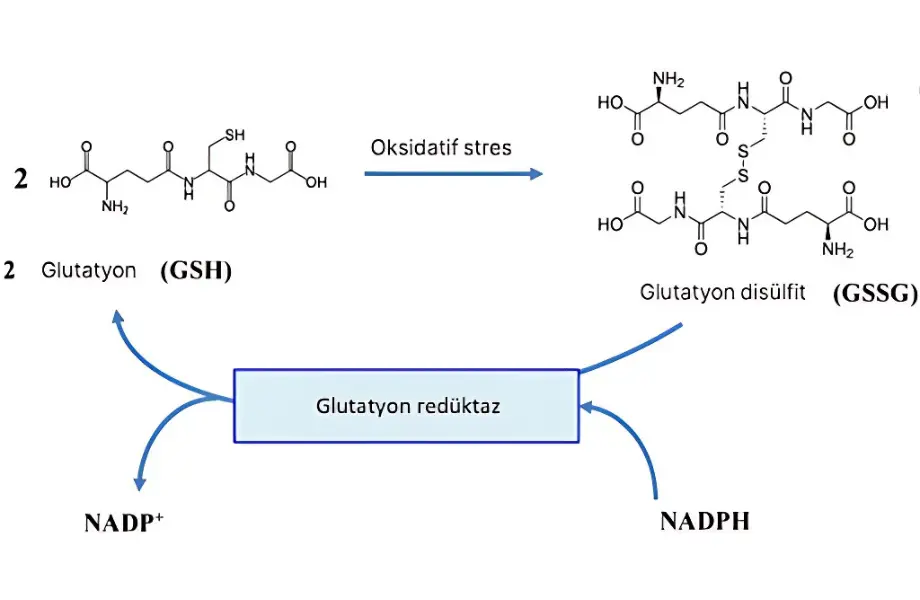
Glutatyon, hücrede indirgenmiş (GSH) ya da oksitlenmiş (GSSG) şeklinde bulunabilir. Bu, hücrenin oksidatif stresine bağlı olarak değişir. Genelde GSH’ın daha fazla oluşu hücrenin daha sağlıklı olduğunu gösterir: örneğin E. coli bakterisinde GSH-GSSG oranı 200’dür. Eğer bu oran GSSG yönünde bozulursa birtakım senaryolar ile oran eski haline döndürülebilir. Bunlardan biri de NADPH (genelde kullanılan) ve NADH (nadiren kullanılan) kullanılarak glutatyon redüktaz enzimi ile GSSG’nin GSH’ye dönüştürülmesidir. [3] [5]
Glutatyonun hidrofilik özelliği
Hidrofili, Yunanca kökenli olup “su” ve “arkadaşlık” sözcüklerinin birleşimidir. Bir molekülün hidrojen bağları kurarak suya bağlanabilme özelliğidir. [12] Glutatyon, oldukça hidrofilik ve biyouyumlu bir molekül olup vücudumuzun birçok bölgesinde görev alır: buna biyotransformasyon sırasında karaciğerdeki lipofilik toksinlere eklenmesi de dahildir. [13]
Glutatyonun streokimyası
L-Konfigürasyonu ve D-Konfigürasyonu olmak üzere iki çeşittir. Bir stereoizomerasyon tipi (enantiyomerlerin alt tipi) olan L- ve D- konfigürasyonları, kiral karbon atomuna sahip molekülün birbiri ile tam örtüşmeyen ayna yansımaları halidir. Moleküllerin kapalı hali bağ zinciri birbirinin aynısı olsa da moleküller birbirerinin aynadaki yansımaları gibidir ve atomların ya da atom gruplarının uzaydaki yönelimleri yüzünden tam olarak örtüşmezler.
Zaten L ve D harfleri Latince kökenli olan “laevus” (solda olan, sola doğru olan) ve “dexter”dan (sağda olan, sağa doğru olan) gelmektedirler. Fischer projeksiyonu denilen yöntem ile üç boyutlu moleküllerin iki boyutlu şekilde yansıtılması işlemi esas alınır. Eğer molekül OH grubu içeriyorsa stereoizomerasyon tipi OH rubunun yerine göre belirlenir. Çoğunlukla amino asitler L- konfigürasyonuna uyarken şekerler ise D-konfigürasyonuna uyar. Ancak bu, moleküllerin sadece tek bir konfigürayon tipine uyacakları anlamına gelmez. Örneğin canlılar için büyük önem arz eden glikoz hem L-glikoz hem de D-glikoz olarak bulunabilir (her ne kadar L-formu nadiren bulunsa da). Doğada bulunan bu enantiyomerlerin varlığını ve önemini kavramak çok önemlidir. Özellikle insan vücudu için de önemli olan amino asit ve karbonhidrat moleküllerindeki izomerasyon, bu moleküllerin ilgili enzimlerin aktif bölgelerince tanınmasını sağlar.
Gelenekselleşmiş anahtar-kilit örneğinde olduğu gibi (eğer el-eldiven ve biren fazla geometrik) anahtarın çalışması için uygun bir kilit gerekir ve bizim durumumuzda kilidin uzaydaki konumu da son derece önemlidir! Yediğiniz gıdalardaki protein ve karbonhidratlardaki izomeriler ve enzimlerinizin aktif bölgeleri uyuşma içerisinde olmasaydı bu gıdaları parçalayıp destek veya enerji elde edemezdiniz. İzomerlerin bir diğer önemli yanı ise iki farklı enantiyomer arasında ciddi tıbbi farklar bulunabileceği için dikkatli olunması gerektiğidir. Örneğin D-etambütol tüberküloza karşı kullanılan bir ilaçken L-etambütolun körlüğe sebep olduğu görülmüştür [14], D-metamfetamin bağımlılık yapıcı ve uzak durulması gereken uyuşturucu bir maddeyken L-metamfetamin ise hakkında klinik ve farmakolojik çalışmalar yapılan bir burun tıkanıklığı gidericisi olan nazaldır. [15]
Glutatyon stereoizomerisi
Glutatyon molekülünün yapısında bulunan glisin, kiral bir karbon atomuna sahip olmadığından dolayı herhangi bir enantiyomere sahip değildir. Ancak sistein ve glutamik asit, amino asit olmalarından dolayı çoğunlukla L- konfigürasyonuna sahiptirler ve bu sebepten doğada L-GSH daha fazla bulunur. Bu yüzden L-GSH üzerine yapılan çalışma sayısı daha fazladır ve bu enantiyomerin canlı organizmalarda inflamasyon önleyici (antienflamatuar) olduğuna dair çalışmalar vardır. [16] [17] D-GSH hakkındaki çalışmaların azlığına dikkat çeken ve bu enantiyomerin de bağışıklık üzerine etkisini inceleyen çalışmalar mevcuttur. [18]
Glutatyonun farmakolojik önemi ve diş hekimliğinde yeri
Farmakolojik önemi
Daha önce değinildiği gibi glutatyon hem hayvanlar hem de bitkiler için çok önemli bir antioksidandır. Hücre döngüsü, bağışıklık sistemi stabilitesi, ağır metal ve hidrojen peroksitlerin, süper-oksit anyonların ve nitrik oksitlerin detoksifikasyonu ve ayrıştırılması, hücresel makromolekülleri reaktif oksijen ve nitrojen türevlerinden (serbest radikallerden) koruma, bazı enzimlere kofaktör olarak katılma gibi birçok işleve sahiptir. [1] [4] [5] [19] [20]
Glutatyonun bu denli önemli bir molekül olması onun tıpta ve diş hekimliğinde kullanımının yaygın olmasını sağlamıştır. Glutatyona dair; enfeksiyon ve iltihaplanmaya karşı direnç, oksidatif stresi azaltmasından dolayı diyabet ve kardiyovasküler hastalıklarda pozitif yönde etki, GSH dengesinin şizofreni ve Alzheimer hastalığı gibi nörolojik hastalıklarda önemi ile ilgili küçük ve büyük çaplı birçok klinik araştırması mevcuttur. [21] [22] [23]
Genel kabul, GSH:GSSG dengesinin doğru sağlanabilmesi için glutatyonun yeteri derecede vücuda alınması gerektiği ve gerekli görülen durumlarda doktor tavsiyesi üzerine diyet veya ek takviyelere başvurulması gerektiği yönündedir. [21] Özellikle ömrü uzattığı ve bu sebeple geriatrik hastalarda (yaşlı bireylerde) kullanımı ve kanser hastası bireylerde kullanımına dair araştırmalar devam etmektedir. [20] [22] [24]
Diş hekimliğinde glutatyonun yeri
Glutatyon daha çok sağlığı pozitif yönde etkileyen bir molekül olsa da hem koruyucu hem de patojenik özelliklerinin olduğu söylenebilir. [25] Özellikle kanser çalışmalarında ve tümör üzerine etkisi tartışmalıdır. Yüksek seviyede glutatyonun kanser hücrelerinde tümörün ilerlemesi ve kemoterapi ilaçlarına karşı direnç geliştirmesi ile ilişkili olduğu görülmüş olsa da günümüzde düşük direnç/yüksek yanıt modelini sağlamaya çalışan glutatyon ile ilişkili tedavi yöntemleri geliştirilmektedir. [21] [26]
Diş hekimliğinde ise yapılan çalışmalar ve glutatyonun etkileri farklılık göstermektedir: Örneğin 6-14 yaş aralığındaki 257 tane Koreli çocukta yapılan bir araştırmada çocukların tükrüklerindeki GSH ve GSSG değerleri ve ayrıca Lactobasillus ile Streptococcus mutants türü bakterilerin (Diş hekimliği alanında günümüzde yapılan çalışmalar çoğunlukla Lactobacillus ve Streptococcus içeren probiyotik kullanımını araştırmaktadır. Bu ürünlerin kullanımına dair olumlu sonuçlar çok sayıda çalışma tarafından ortaya konmuştur. [27]) seviyeleri ölçülmüş ve GSH değerleri ile diş çürükleri arasında bir ilişki bulunmuştur. Yapılan bu çalışma ile Lactobacillus ve Streptococcus bakterileri ve diş çürüklerinin varlığında GSH’ın anlamlı düzeyde arttığı ve bu sebeple GSH’ın kariyojenik bakterileri ve diş çürüklerini saptamada biyobelirteç olarak kullanılabileceğine değinilmiştir. [28] Ancak bu çalışmada, diğer birçok çalışmanın aksine uyarılmış tükrük kullanılmış ve (bu sefer diğer birçok çalışmayla benzer şekilde) diş çürüklerinin derinliği es geçilerek sadece diş çürük sayısı verilmiştir. [29]
Yapılan başka iki çalışmada ise diş çürüğü tedavisinde kullanılan ancak sonrasında istenmeyen renk değişikliklerine sebep olan (siyahlaşan) bir gümüş bileşiği olan gümüş diamin florür (GDF) ve GDF’ye ayrı ayrı glutatyon (GSH) ve potasyum iyodür (KI) eklenmesi sonucu olan değişimler ele alınmıştır. [30] [31] Çalışmalardan birinde glutatyon biyomolekülünün, GDF uygulaması sonrası diş yüzeyindeki renk değişikliklerini, özellikle minede ve daha az oranda da dentin üzerinde azaltıcı etkisinin olduğu, [30] diğerinde ise (mevcut sınırlamalar dahilinde) GDF çözeltisine ağırlıkça %5 GSH eklenmesinin, SDF’nin neden olduğu renk bozulması üzerinde önemli bir etkisi olmadığı ancak SDF’nin yeniden mineralizasyon potansiyeli üzerinde küçük bir etkisi olabileceği görülmüştür. [31]
Bu çalışmalardan anlaşılabileceği üzere glutatyon biyomolekülünün sadece diş çürükleri üzerine olan etkisiyle ilgili bile birbirinden farklı çalışmalar ve sonuçlar mevcut. Bu sebeple kesin yargılara varamasak da bağışıklık sistemi için çok önemli olan bu biyomolekül ile ilgili çalışmalar devam etmektedir ve yeni tedavi yöntemleri geliştirilmeye çalışılmaktadır.
- AKADEMİK DERGİ Noctor, G., Queval, G., Mhamdi, A., Chaouch, S., & Foyer, C. H. (2011). Glutathione. The Arabidopsis Book, 9, 1–32. [The Arabidopsis Book]
- WEBSİTE American Chemical Society. (2017, May 29). Glutathione. American Chemical Society. [American Chemical Society]
- SÖZLÜK YAZISI Wikipedia Turkish. (2021). Glutatyon. In Wikipedia Turkish. [Wikipedia Turkish]
- AKADEMİK DERGİ Townsend, D. M., Lushchak, V. I., & Cooper, A. J. (2014). A comparison of reversible versus irreversible protein glutathionylation. Advances in Cancer Research, 177–198. [Advances in Cancer Research]
- AKADEMİK DERGİ Cassier-Chauvat, C., Marceau, F., Farci, S., Ouchane, S., & Chauvat, F. (2023). The Glutathione System: A Journey from Cyanobacteria to Higher Eukaryotes. Antioxidants, 12(6), 1199. [Antioxidants]
- AKADEMİK DERGİ Raftos, J. E., Whillier, S., & Kuchel, P. W. (2010). Glutathione synthesis and turnover in the human erythrocyte. Journal of Biological Chemistry, 285(31), 23557–23567. [Journal of Biological Chemistry]
- WEBSİTE The Nobel Prize. (n.d.). Vincent du Vigneaud Facts. The Nobel Prize. [The Nobel Prize]
- WEBSİTE Harvard Health. (2019, January 31). Understanding antioxidants. Harvard Health. [Harvard Health]
- AKADEMİK DERGİ Karabulut, H., & Gülay, M. Ş. (2016). ANTİOKSİDANLAR. Mehmet Akif Ersoy Üniversitesi Veteriner Fakültesi Dergisi, 1(1), 65. [Mehmet Akif Ersoy Üniversitesi Veteriner Fakültesi Dergisi]
- SÖZLÜK YAZISI Wikipedia Turkish. (2009). Radikal (kimya). In Wikipedia Turkish. [Wikipedia Turkish]
- AKADEMİK DERGİ Muraoka, M., Ohno, M., Nakai, T., Matsuura, H., Nagano, K., Arai, M., Hirata, Y., Uyama, H., & Hirata, K. (2022). Gamma-Glutamylcysteine Production Using Phytochelatin Synthase-Like Enzyme Derived from Nostoc sp. Covalently Immobilized on a Cellulose Carrier. Biological and Pharmaceutical Bulletin, 45(8), 1191–1197. [Biological and Pharmaceutical Bulletin]
- SÖZLÜK YAZISI Wikipedia Turkish. (2007). Hidrofili. In Wikipedia Turkish. [Wikipedia Turkish]
- WEBSİTE PubChem. (n.d.). Glutathione. PubChem. [PubChem]
- AKADEMİK DERGİ Chhabra, N., Aseri, M., & Padmanabhan, D. (2013). A review of drug isomerism and its significance. International Journal of Applied and Basic Medical Research, 3(1), 16. [International Journal of Applied and Basic Medical Research]
- AKADEMİK DERGİ Mendelson, J. E., McGlothlin, D., Harris, D. S., Foster, E., Everhart, T., Jacob, P., & Jones, R. T. (2008). The Clinical Pharmacology of Intranasal L-Methamphetamine. BMC Clinical Pharmacology, 8(1). [BMC Clinical Pharmacology]
- AKADEMİK DERGİ Folkers, K., Dahmen, J., Ohta, M., Stepien, H., Leban, J., Sakura, N., Lundanes, E., Rampold, G., Patt, Y., & Goldman, R. (1980). Isolation of glutathione from bovine thymus and its significance to research relevant to immune systems. Biochemical and Biophysical Research Communications, 97(2), 590–594. [Biochemical and Biophysical Research Communications]
- AKADEMİK DERGİ Utsugi, M., Dobashi, K., Koga, Y., Shimizu, Y., Ishizuka, T., Iizuka, K., Hamuro, J., Nakazawa, T., & Mori, M. (2002). Glutathione redox regulates lipopolysaccharide-induced IL-12 production through p38 mitogen-activated protein kinase activation in human monocytes: role of glutathione redox in IFN-γ priming of IL-12 production. Journal of Leukocyte Biology, 71(2), 339–347. [Journal of Leukocyte Biology]
- AKADEMİK DERGİ Kim, S., Ko, W., Han, G., Lee, D., Lee, Y., Sheen, S., Hong, J., & Sohn, S. (2021). Chirality-Dependent Anti-Inflammatory Effect of Glutathione after Spinal Cord Injury in an Animal Model. Pharmaceuticals, 14(8), 792. [Pharmaceuticals]
- WEBSİTE Pizzorno, J. (2014, February 1). Glutathione! PubMed. [PubMed]
- AKADEMİK DERGİ Marí, M., Morales, A., Colell, A., García-Ruiz, C., & Fernández-Checa, J. C. (2009). Mitochondrial glutathione, a key survival antioxidant. Antioxidants and Redox Signaling, 11(11), 2685–2700. [Antioxidants and Redox Signaling]
- AKADEMİK DERGİ Novelli, A., & Bianchetti, A. (2022). Glutathione: pharmacological aspects and implications for clinical use. Geriatric Care, 8(2). [Geriatric Care]
- AKADEMİK DERGİ Ballatori, N., Krance, S. M., Notenboom, S., Shi, S., Tieu, K., & Hammond, C. L. (2009). Glutathione dysregulation and the etiology and progression of human diseases. Biological Chemistry, 390(3), 191–214. [Biological Chemistry]
- AKADEMİK DERGİ Gu, F., Chauhan, V., & Chauhan, A. (2014). Glutathione redox imbalance in brain disorders. Current Opinion in Clinical Nutrition & Metabolic Care, 18(1), 89–95. [Current Opinion in Clinical Nutrition & Metabolic Care]
- AKADEMİK DERGİ Lu, S. C. (2012). Glutathione synthesis. Biochimica Et Biophysica Acta (BBA) – General Subjects, 1830(5), 3143–3153. [Biochimica Et Biophysica Acta (BBA) – General Subjects]
- AKADEMİK DERGİ Kennedy, L., Sandhu, J. K., Harper, M., & Cuperlovic-Culf, M. (2020). Role of glutathione in cancer: From mechanisms to therapies. Biomolecules, 10(10), 1429. [Biomolecules]
- AKADEMİK DERGİ Wang, J., & Yi, J. (2008c). Cancer cell killing via ROS: To increase or decrease, that is the question. Cancer Biology & Therapy, 7(12), 1875–1884. [Cancer Biology & Therapy]
- AKADEMİK DERGİ Alkaya, B., & Uçak, O. (2017). Streptecoccus ve Lactobacillus Cinsi Probiyotiklerin Diş Hekimliğinde Kullanımı. Turkiye Klinikleri Periodontology-Special Topics, 3(1), 10-14. [Turkiye Klinikleri Periodontology-Special Topics]
- AKADEMİK DERGİ Han, D., Kim, M., Jun, E., & Kim, J. (2013). The role of glutathione metabolism in cariogenic bacterial growth and caries in Korean children. Archives of Oral Biology, 58(5), 493–499. [Archives of Oral Biology]
- AKADEMİK DERGİ De Sousa Né, Y. G., Lima, W. F., Mendes, P. F. S., Baia-Da-Silva, D. C., Bittencourt, L. O., Nascimento, P. C., De Souza-Rodrigues, R. D., Paranhos, L. R., Martins-Júnior, P. A., & Lima, R. R. (2023). Dental Caries and Salivary Oxidative Stress: Global Scientific Research Landscape. Antioxidants, 12(2), 330. [Antioxidants]
- AKADEMİK DERGİ Sayed, M., Matsui, N., Hiraishi, N., Nikaido, T., Burrow, M. F., & Tagami, J. (2018). Effect of Glutathione Bio-Molecule on Tooth Discoloration Associated with Silver Diammine Fluoride. International Journal of Molecular Sciences, 19(5), 1322. [International Journal of Molecular Sciences]
- AKADEMİK DERGİ Cömert, H., & Olmez, A. (2024). Effects of glutathione and potassium iodide on silver diamine fluoride application on remineralisation and colour change in dentine caries of primary teeth: an in vitro study. European Archives of Paediatric Dentistry. [European Archives of Paediatric Dentistry]
APA 7: Kaplan, B. Y. (2024, December 16). Glutatyon Nedir? PerEXP Teamworks. [Makale Bağlantısı]